آزمایشهای مرتبط با انواع سرطانهای خون
- سرطانهای خون (Blood Cancers) گروهی از بدخیمیهای با منشأ سلولهای خونساز هستند که شامل لوسمی (Leukemia)، لنفوم (Lymphoma) و میلوما (Myeloma) میشوند. این بیماریها بهدلیل تغییرات ژنتیکی و مولکولی در سلولهای بنیادی مغز استخوان ایجاد میشوند و منجر به رشد کنترلنشدهی سلولهای غیرطبیعی خونی میگردند.
در سالهای اخیر، پیشرفت در ژنتیک مولکولی و سیتوژنتیک (Cytogenetics) باعث تحول چشمگیری در تشخیص، طبقهبندی و درمان این بیماریها شده است. بر اساس طبقهبندی جدید سازمان جهانی بهداشت (WHO 2022)، بسیاری از انواع لوسمیها و لنفومها بر اساس تغییرات ژنی خاص (مانند BCR-ABL1، FLT3، NPM1، JAK2، TP53 و سایر مارکرها) تعریف میشوند. تستهای ژنتیکی و مولکولی نقش حیاتی در تعیین نوع دقیق بیماری، پیشآگهی (Prognosis) و انتخاب درمان هدفمند (Targeted Therapy) دارند. امروزه آزمایشهایی مانند PCR، FISH، NGS و فلوسایتومتری (Flow Cytometry) بخش جداییناپذیر از ارزیابی بیماران مبتلا به لوسمی و سایر بدخیمیهای خونی هستند. همچنین کاریوتایپ مغز استخوان (Bone Marrow Karyotyping) یکی از اولین و بنیادیترین تستها در روند تشخیص لوسمیها و سایر بدخیمیهای خون است. در این روش، با بررسی تعداد و ساختار کروموزومها در سلولهای مغز استخوان، میتوان تغییرات کروموزومی نظیر ترانسلوکاسیونها، حذفها، افزایشها یا اینورژنها را شناسایی کرد.
در آزمایشگاه کریمینژاد - نجمآبادی، تمامی تستهای تخصصی مولکولی و ژنتیکی مرتبط با لوسمی و سرطانهای خون بر اساس جدیدترین استانداردهای بینالمللی انجام میشود. برای مشاهده لیست کامل تستها و پنلها، به بخش زیر مراجعه کنید.
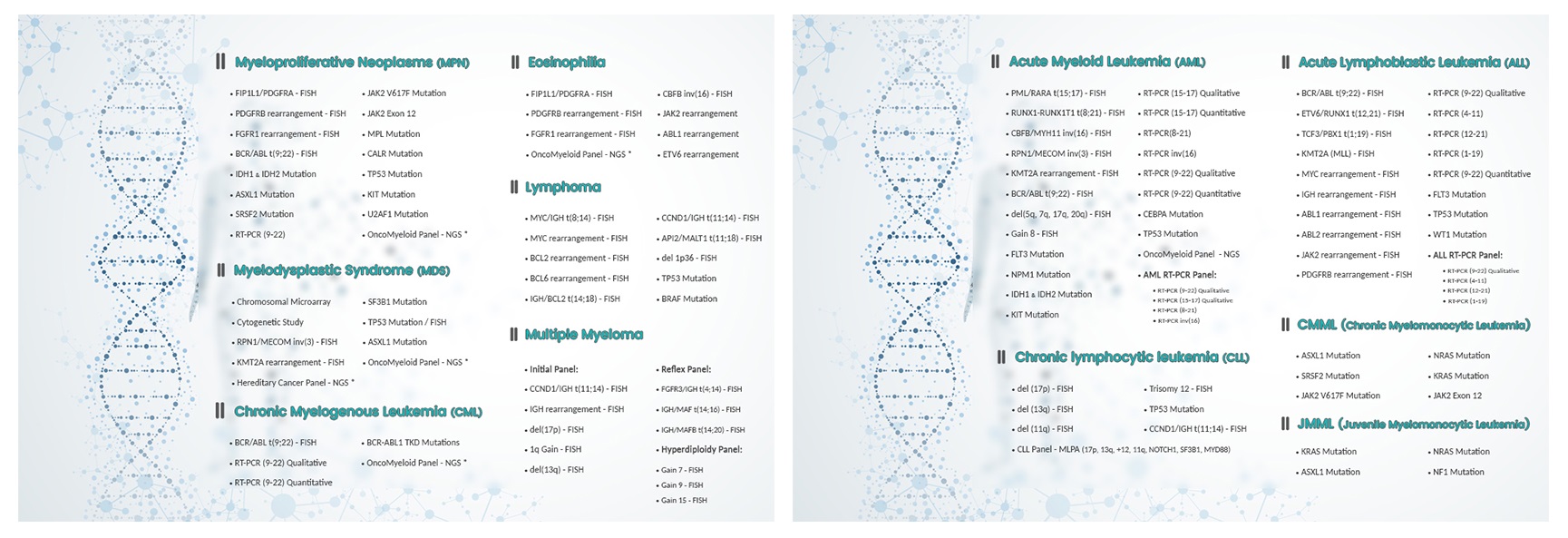

۱. Myeloproliferative Neoplasms (MPN)
در نئوپلاسمهای میلوپرولیفراتیو، تشخیص مولکولی نقشی کلیدی در افتراق انواع بیماری و انتخاب درمان هدفمند دارد.
مهمترین مارکرهای مولکولی عبارتاند از:
• JAK2 V617F و JAK2 Exon 12 (تشخیص PV و سایر MPNها)
• MPL و CALR (در موارد JAK2 منفی)
• BCR/ABL1 (t9;22) - FISH برای افتراق از CML
• ASXL1، TP53، U2AF1 و SRSF2 Mutations برای پیشآگهی
• OncoMyeloid NGS Panel جهت شناسایی جامع موتاسیونها
2. Acute Myeloid Leukemia (AML)
لوسمی میلوئید حاد (AML) یکی از شایعترین لوسمیهای بالغین است که با تجمع سلولهای نابالغ میلوئیدی در مغز استخوان و خون مشخص میشود. در طبقهبندی جدید WHO 2022، AML بر اساس جهشهای ژنتیکی و بازآراییهای مولکولی تقسیمبندی میشود، نه صرفاً بر پایه مورفولوژی. مهمترین مارکرهای مولکولی در تشخیص و پیشآگهی AML عبارتاند از:
• PML/RARA t(15;17) → تشخیص APL
• RUNX1-RUNX1T1 t(8;21) و CBFB-MYH11 inv(16) → AML با پیشآگهی مطلوب
• FLT3، NPM1، CEBPA، IDH1/2، TP53، KIT → تعیین ریسک و انتخاب درمان هدفمند
• BCR/ABL1 (t9;22) FISH و RT-PCR → افتراق از CML در مرحله بلاستیک
• OncoMyeloid Panel - NGS → ارزیابی جامع ۵۰+ ژن مرتبط با AML
نتیجهی دقیق تستهای مولکولی در AML نقش تعیینکنندهای در انتخاب درمانهایی مانند مهارکنندههای FLT3، IDH1/2 و داروهای اپیژنتیک دارد.
3. Acute Lymphoblastic Leukemia (ALL)
لوسمی لنفوبلاستیک حاد (ALL) بیشتر در کودکان دیده میشود اما در بالغین نیز با الگوهای ژنتیکی متفاوت رخ میدهد. تشخیص دقیق ALL امروزه بر پایهی ترکیبی از فلوسایتومتری، سیتوژنتیک و تستهای مولکولی (PCR و FISH) انجام میشود. مهمترین مارکرهای مولکولی و کروموزومی در ALL عبارتاند از:
• BCR/ABL1 (t9;22) → فیلادلفیا مثبت ALL (Ph+)
• ETV6/RUNX1 t(12;21) → فرم با پیشآگهی مطلوب در کودکان
• TCF3/PBX1 t(1;19) → فرم با ریسک متوسط
• KMT2A (MLL) Rearrangement، MYC، IGH، JAK2، PDGFRB، TP53، WT1
• RT-PCR Panel (شامل t(9;22)، t(4;11)، t(12;21)، t(1;19)) برای تشخیص سریع و پایش درمان
نتایج ژنتیکی در ALL تعیینکننده نوع درمان هستند، از جمله استفاده از مهارکنندههای BCR-ABL و CAR-T Cell Therapy در موارد خاص.
4. Chronic Myelogenous Leukemia (CML)
تشخیص قطعی CML بر پایه شناسایی ترانسلوکاسیون BCR-ABL1 (t9;22) است.
• RT-PCR (Qualitative / Quantitative) برای تشخیص و پایش پاسخ درمانی
• FISH برای BCR/ABL1
• TKD Mutation Testing جهت بررسی مقاومت دارویی به TKIها
5. Chronic Lymphocytic Leukemia (CLL)
در CLL، تستهای مولکولی برای تعیین پیشآگهی و انتخاب درمان ضروری هستند:
• del(17p)/TP53 mutation → پیشآگهی ضعیف، مقاومت به شیمیدرمانی
• Trisomy 12، del(11q)، del(13q) → تعیین ریسک متوسط یا پایینتر
• IGH/CCND1 Rearrangement → افتراق از لنفوم مانتسل
• CLL MLPA Panel (شامل NOTCH1، SF3B1، MYD88 و ...)
6. Myelodysplastic Syndrome (MDS)
تشخیص MDS نیازمند شناسایی تغییرات ژنتیکی کلیدی است:
• SF3B1، TP53، ASXL1 Mutations → تأثیرگذار بر پیشآگهی
• Chromosomal Microarray و Cytogenetic Study → بررسی تغییرات ساختاری
• RPN1/MECOM inv(3) و KMT2A rearrangement → زیرگروههای پرخطر
• OncoMyeloid NGS Panel برای تشخیص جامع
7. Lymphoma
در لنفومها، بررسی بازآراییهای ژنی برای تعیین نوع دقیق تومور حیاتی است:
• MYC, BCL2, BCL6 rearrangements (FISH)
• CCND1/IGH t(11;14) → Mantle Cell Lymphoma
• API2/MALT1 t(11;18) → MALT Lymphoma
• TP53، BRAF Mutations → تعیین مسیرهای درمانی هدفمند
8. Multiple Myeloma
تستهای مولکولی برای تعیین ریسک سیتوژنتیکی و انتخاب رژیم درمانی ضروریاند:
• CCND1/IGH t(11;14)، IGH Rearrangements، del(17p)
• Gain 1q، del(13q)
• FGFR3/IGH t(4;14) و IGH/MAF t(14;16)
9. CMML و JMML
در لوکمیهای مونوسیتیک بالغ و جوانان:
• ASXL1، NRAS، KRAS، SRSF2، NF1 Mutations
• JAK2 V617F و Exon 12 Mutations
